 Leitlinien Essentials
Leitlinien Essentials

DGRh – Leitlinienübersicht
https://www.dgrh.de/lesen/leitlinien/leitlinien-dgrh/
DGRh – Empfehlungen
https://www.dgrh.de/lesen/empfehlungen/
DGRh – Klassifikationskriterien
https://www.dgrh.de/behandeln/klassifikation/klassifikationskriterien
EULAR – Recommendations Home
https://www.eular.org/recommendations-home
EULAR – Recommendations for Management
https://www.eular.org/recommendations-management
EULAR – Classification / Diagnosis / Response Criteria
https://www.eular.org/recommendations-classification-response-criteria-diagnostic
EULAR/ACR – gemeinsame Empfehlungen und Kriterienprojekte
https://www.eular.org/recommendations-eular-acr
ACR – Clinical Practice Guidelines
https://rheumatology.org/clinical-practice-guidelines
ACR – Kriterien
https://rheumatology.org/criteria
ASAS – axSpA-Empfehlungen
https://www.asas-group.org/asas-eular-recommendations-for-the-management-of-axspa-2022-update/
https://www.asas-group.org/asas-recommendations-for-requesting-and-reporting-imaging-in-patients-with-suspected-axial-spondyloarthritis/
GRAPPA – PsA Toolkit Resources
https://psa.guidelinecentral.com/toolkit-resources/
ERS/EULAR – CTD-ILD-Leitlinie
https://publications.ersnet.org/content/erj/67/1/2402533
https://publications.ersnet.org/content/erj/67/1/2501973
AWMF/DGRh – Diagnostik und Therapie des adulten Still-Syndroms 2023
Übersicht https://register.awmf.org/de/leitlinien/detail/060-011
Langfassung https://register.awmf.org/assets/guidelines/060-011l_S2e_Diagnostik-Therapie-des-adulten-Still-Syndroms-AOSD_2023-11.pdf
AWMF/DGRh – Diagnostik und Therapie der ANCA-assoziierten Vaskulitiden 2024
Übersicht https://register.awmf.org/de/leitlinien/detail/060-012
Langfassung https://register.awmf.org/assets/guidelines/060-012l_S3_Diagnostik-Therapie-ANCA-assoziierten_Vaskulitiden_2024-08_2_01.pdf
EULAR – Management of ANCA-associated vasculitis (2022 update)
https://ard.bmj.com/content/83/1/30
Granulomatose mit Polyangiitis (GPA), ACR/EULAR 2022
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/art.41986
Mikroskopische Polyangiitis (MPA), ACR/EULAR 2022
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/art.41983
Eosinophile Granulomatose mit Polyangiitis, (EGPA) ACR/EULAR 2022
https://ard.eular.org/article/S0003-4967(24)09565-7/abstract
ACR – Vasculitis Guideline Hub
https://rheumatology.org/vasculitis-guideline
ACR/VF – Guideline for Giant Cell Arteritis and Takayasu Arteritis
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/acr.24632
ACR/VF – Guideline for ANCA-associated vasculitis
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/acr.24634
ASAS/EULAR – Management of axSpA (2022 update)
https://ard.bmj.com/content/82/1/19
AWMF/DGRh – S3 Axiale Spondyloarthritis inklusive Morbus Bechterew und Frühformen 2018 (in Überarbeitung)
https://register.awmf.org/de/leitlinien/detail/060-003
ACR/SAA/SPARTAN – Empfehlungen zu AS und nr-axSpA (2019)
https://pmc.ncbi.nlm.nih.gov/articles/PMC6764882/
ASAS – Klassifikationskriterien für axiale SpA
Originalpublikation https://pubmed.ncbi.nlm.nih.gov/19297344/
Deutsch https://pubmed.ncbi.nlm.nih.gov/19680669/
ASAS – Klassifikationskriterien für periphere SpA
https://pubmed.ncbi.nlm.nih.gov/21109520/
AWMF/DGRh – Diagnostik und Therapie der Gicht
Übersicht https://register.awmf.org/de/leitlinien/detail/060-005
Langfassung https://register.awmf.org/assets/guidelines/060-005l_S3_Diagnostik-Therapie-Gicht_2025-01.pdf
ACR – 2020 Guideline for the Management of Gout
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/acr.24180
ACR/EULAR – 2015 Klassifikationskriterien für Gicht
https://ard.eular.org/article/S0003-4967(24)02543-3/fulltext
ACR/EULAR – 2023 Klassifikationskriterien für CPPD
https://pubmed.ncbi.nlm.nih.gov/37494275/
2022 ACR/EULAR – Giant Cell Arteritis (GCA)
https://ard.eular.org/article/S0003-4967(24)08730-2/fulltext
2022 ACR/EULAR – Takayasu-Arteriitis (TAK)
https://ard.eular.org/article/S0003-4967(24)08731-4/fulltext
AWMF/DGRh – Management der Großgefäßvaskulitiden 2020 (in Überarbeitung)
Übersicht https://register.awmf.org/de/leitlinien/detail/060-007
ERS/EULAR – CTD-ILD Clinical Practice Guideline
https://publications.ersnet.org/content/erj/67/1/2402533
ACR/CHEST – Screening/Monitoring von SARD-ILD
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/art.42860
ACR/CHEST – Treatment von SARD-ILD
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/art.42861
ACR – Juvenile Idiopathic Arthritis Guideline Hub
https://rheumatology.org/juvenile-idiopathic-arthritis-guideline
ACR – 2021 Guideline for JIA
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/acr.24839
ACR/EULAR – 2017 Klassifikationskriterien für adulte und juvenile IIM
https://pmc.ncbi.nlm.nih.gov/articles/PMC5736307/
Myositissyndrome S2k 2024
Übersicht: AWMF Leitlinienregister
Langfassung: https://register.awmf.org/assets/guidelines/030-
054l_S2k_Myositissyndrome_2024-10-verlaengert.pdf
International Guideline for Idiopathic Inflammatory Myopathy-Associated Cancer Screening
https://www.nature.com/articles/s41584-023-01045-w
Differentialdiagnose Myalgien:
https://register.awmf.org/assets/guidelines/030-051l_S1_Diagnostik-Differentialdiagnose-
Adaptiert nach: S2e-Leitlinie zur Behandlung der Polymyalgia rheumatica, Update 2024 (AWMF 60/006, DGRh/ÖGR/SGR)
AWMF/DGRh – Behandlung der Polymyalgia rheumatica
Übersicht https://register.awmf.org/de/leitlinien/detail/060-006
Langfassung https://register.awmf.org/assets/guidelines/060-006l_S2e_Behandlung-der-Polymyalgia-rheumatica_2025-04.pdf
ACR/EULAR – 2012 Klassifikationskriterien für PMR
https://pubmed.ncbi.nlm.nih.gov/22388996/
EULAR/ACR – 2015 Empfehlungen zum Management der PMR
https://ard.eular.org/article/S0003-4967(24)02544-5/fulltext
Entzündlich-rheumatische Erkrankung ≥ 50 Lj.; Frauen ~3× häufiger
Zweithäufigste entzündlich-rheumatische Erkrankung im Alter
Spektrum mit Riesenzellarteriitis (RZA)
~20 % PMR + RZA gleichzeitig
~50 % der RZA-Patient:innen zeigen PMR-Symptome
Akuter Beginn von Schmerzen mit entzündlichem Charakter& Steifigkeit in Schulter-/Beckengürtel
Ausgeprägte Morgensteifigkeit
Häufig: Fatigue, Gewichtsverlust, subfebrile Temperaturen, Nachtschweiß
Erhöhte Entzündungsparameter (CRP und BSG)
Immer an RZA denken: Kopfschmerz, Visus, Kauschmerz
Ausschluss anderer Ursachen (entzündlich, endokrin, infektiös, neoplastisch)
Labor (auswählen): CRP, BSG, BB, Leber/Niere, Glukose, Ca, AP, Vit D, TSH, CK
Autoantikörper: RF, anti-CCP, ANA, ANCA
Bildgebung:
Schulter- und Hüft-Arthrosonographie
Gefäßultraschall bei RZA-Verdacht
Knochendichtemessung (Baseline)
Ergänzend: Röntgen-Thorax, Abdomen-Sonographie
Bei Vaskulitisverdacht: PET-CT, MRT oder kontrastverstärkte CT
Glukokortikoide (GC) – Erstlinientherapie
Start sofort nach Diagnosesicherung
Initial: 15–25 mg Prednison-Äquivalent/d (Individuelle Entscheidung zur GC-Initialdosis nach Einbezug von Begleiterkrankungen und Begleitmedikationen)
Morgendliche Einzeldosis
GC-Reduktion
Ziel: 10 mg/Tag nach 4–8 Wochen
Weiteres Vorgehen: Reduktion um ca. 1 mg alle 4 Wochen
Bei Rezidiv: Erhöhung auf die Prä-Rezidiv-Dosis und anschließend erneute schrittweise Reduktion
Behandlungsdauer der GC-Therapie
GC-Monotherapie: ≤ 1 Jahr
GC + Begleitende Biologika-Therapie: max. 16 Wochen
GC + Begleitende MTX-Therapie: 6-8 Monate
Sarilumab (zugelassen)
Einsatz: zusätzlich zu GC
Empfohlen bei rezidivierender PMR
Kann erwogen werden bei neuer PMR + hohem GC-Risikoprofil
Tocilizumab (Off-Label)
Nur Zusatz zu GC
Gleiche klinische Indikationen wie Sarilumab, aber Off-Label
Alternativen zu IL-6Ri (Off-Label)
Methotrexat (MTX)
Rituximab
Keine Zulassung für PMR (Off-Label-Use)
Einsatz als GC-sparende Option, wenn IL-6-Rezeptorblockade nicht geeignet ist z. B. bei Nadelphobie oder vorbestehender Divertikulitis
Bis Remission: alle 1–4 Wochen
Stabile Remission: alle 3–6 Monate
Nach Absetzen: individuell
Monitoring: Symptome, BSG/CRP, GC-Nebenwirkungen, Komorbiditäten
Bei älteren / gebrechlichen Patient*innen:
Individualisiertes Übungsprogramm (Muskelkraft, Mobilität, Sturzprävention)
Basierend auf: EULAR Guideline - 2022 Update
EULAR – Management of psoriatic arthritis with pharmacological therapies (2023 update)
https://ard.bmj.com/content/83/6/706
AWMF/DGRh – S3 Diagnosestellung und medikamentöse Therapie der Psoriasis-Arthritis (2026 erwartet)
https://register.awmf.org/de/leitlinien/detail/060-013
ACR/NPF – 2018 Guideline for the Treatment of Psoriatic Arthritis
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/art.40726
GRAPPA – Toolkit Resources
https://psa.guidelinecentral.com/toolkit-resources/
GRAPPA – Treatment Recommendations (2021 update)
https://www.nature.com/articles/s41584-022-00798-0
CASPAR – Klassifikationskriterien für PsA
https://pubmed.ncbi.nlm.nih.gov/16871531/
csDMARD
Methotrexate
Leflunomide
Sulfasalazine
bDMARD
TNF
Adalimumab
Certolizumab
Etanercept
Infliximab
Golimumab
IL-12/23
Ustekinumab
IL-17A
Ixekizumab
Secukinumab
IL-17A/F
Bimekizumab
IL-23-p19
Guselkumab
Risankizumab
CTLA4
Abatacept
tsDMARD
PDE4
Apremilast
JAK
Tofacitinib.
Upadacitinib.
Ziel ist die Remission
Nach Therapie(-umstellung): Besserung nach 3 Monaten, Remission oder geringe Krankheitsaktivität nach 6 Monaten
Symptom Mangement: NSAR oder lokale Steroidinfiltrationen
Polyarthritis oder Monarthritis/Oligoarthritis mit schlechten Prognosefaktoren (Strukturelle Schäden, erhöhte Entzündungsparameter, Daktylitis, Nagelbeteiligung): csDMARDS kurzfristig beginnen. MTX bevorzugen bei Hautbeteiligung.
Periphere Arthritis mit unzureichendem Ansprechen auf mindestens ein csDMARD: bDMARDs
Periphere Arthritis mit unzureichendem Ansprechen auf mindestens ein bDMARD oder wenn bDMARD nicht sinnvoll: JAKi können erwogen werden – Cave: Sicherheitshinweise
Milde Erkrankung und unzureichendes Ansprechen auf mindestens ein csDMARD und wenn weder ein bDMARD oder ein JAKi sinnvoll sind: PDE4 Inhibitoren können erwogen werden.
Axiale Beteiligung mit unzureichendem Ansprechen auf NSAR: IL17A(/F)i, TNFi, JAKi
Relevante Hautbeteiligung: IL17A/F oder IL23i oder IL12/23
Uveitis: TNFi
Chronisch Entzündliche Darmerkrankungen: TNFi, IL23i, IL12/23i
Bei unzureichendem Ansprechen oder Unverträglichkeit: Wechsel auf ein anderes bDMARD oder JAKi, inkl. ein Wechsel innerhalb der Klasse.
Anhaltende Remission: Tapering des bDMARD kann erwogen werden (Cave: Off-Label)
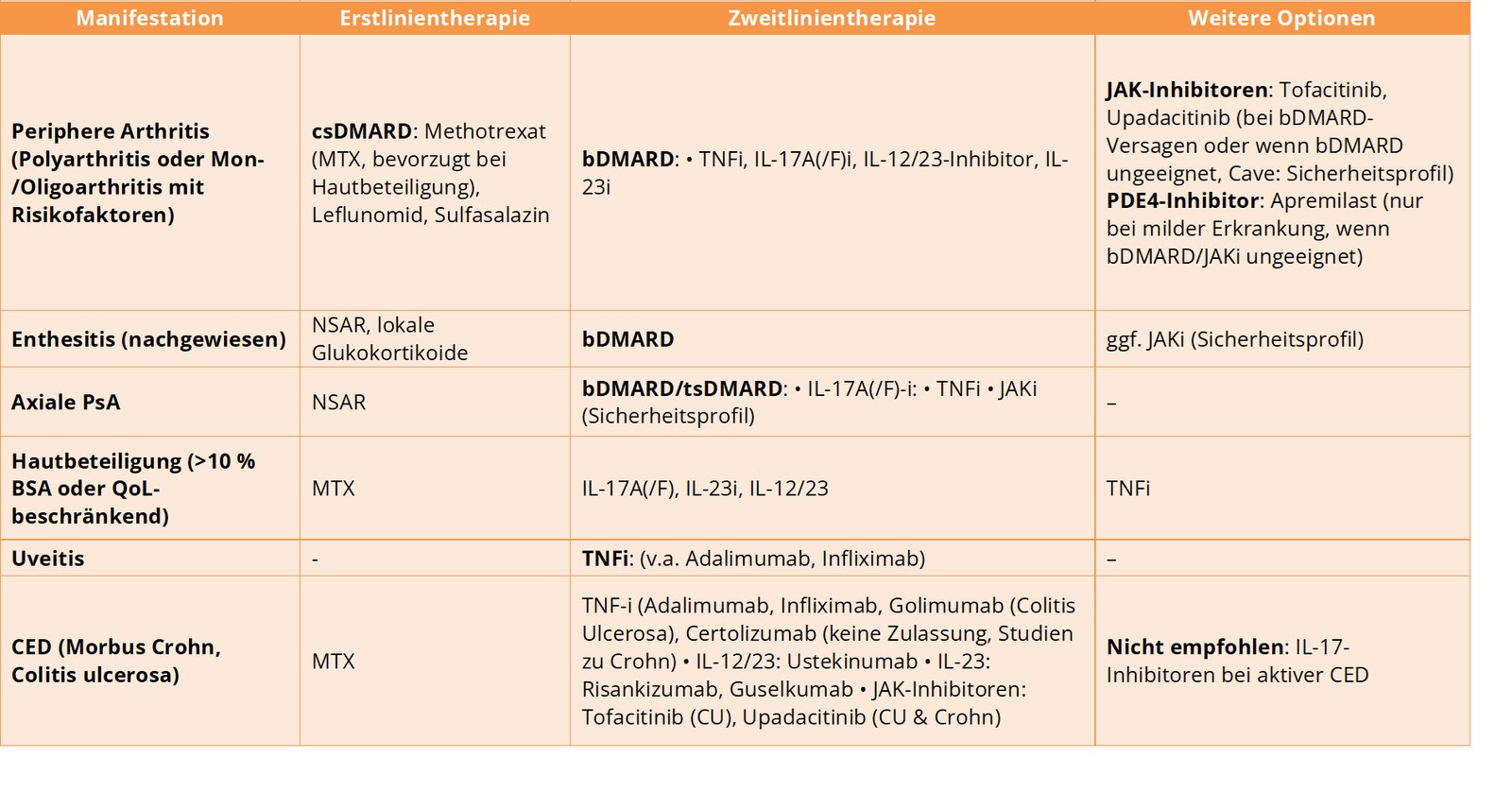
Adaptiert nach EULAR 2022, ACR 2021, AWMF/DGrh-Leitlinien und aktueller Evidenz zu EULAR/ACR 2010-Kriterien
AWMF/DGRh – S3 Therapie der rheumatoiden Arthritis mit krankheitsmodifizierenden Medikamenten 2018 (in Überarbeitung)
Übersicht https://register.awmf.org/de/leitlinien/detail/060-004
Langfassung https://register.awmf.org/assets/guidelines/060-004l_S3_KF_Therapie-rheumatoide-Arthritis-krankheitsmodifizierende-Medikamenten_202-02.pdf
EULAR – Management of rheumatoid arthritis (2022 update)
https://ard.eular.org/article/S0003-4967(24)08619-9/fulltext
DGRh – Management der frühen rheumatoiden Arthritis 2020
https://link.springer.com/content/pdf/10.1007/s00393-020-00775-6.pdf
ACR – Rheumatoid Arthritis Guideline
https://rheumatology.org/rheumatoid-arthritis-guideline
ACR – 2021 Guideline for the Treatment of Rheumatoid Arthritis
https://pmc.ncbi.nlm.nih.gov/articles/PMC9273041/
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/acr.24596
ACR/EULAR – 2010 Klassifikationskriterien für RA
https://ard.eular.org/article/S0003-4967%25252824%25252919350-8/fulltext
Klassifikationskriterien-Rechner https://www.my.crf.one/de/Public/Index/7061
Konventionelle Synthetische Disease Modifying Antirheumatic Drugs (csDMARDS)
Methotrexat (MTX)
Leflunomid
Sulfasalazin
Biologika (bDMARDs)
TNF-Inhibitoren: Adalimumab, Etanercept, Infliximab, Golimumab, Certolizumab
IL-6-Rezeptor-Antagonisten: Tocilizumab, Sarilumab
CTLA-4-Ig: Abatacept
B-Zell-Depletion: Rituximab
JAK-Inhibitoren (tsDMARDs)
Baricitinib
Filgotinib
Tofacitinib
Upadacitinib
Frühe Diagnose und Therapiebeginn entscheidend
Eine DMARD Therapie soll begonnen werden
csDMARDs (Methotrexat als Standard)
Methotrexat: Erstlinientherapie
Startdosis: 15mg wöchentlich (ggf. Steigerung bis 25mg/d), bei > 15mg bevorzugt s.c. wegen verminderter Aufnahme
Folsäure-Supplementation (5-10mg 24h nach MTX Gabe)
Alternativen: Leflunomid (20mg/d), Sulfasalazin (2g/d)
Ergänzende Therapie mit Glucokortikoiden (Bis 30mg Prednisolonäquivalent/d), Reduktion auf Low-Dose innerhalb von 8 Wochen, Gesamtdauer: 3-6 Monate).
Intraartikuläre Steroidgabe möglich
Treat to Target:
Therapieanpassung alle 3 Monate, wenn keine deutliche Besserung bzw. nach 6 Monaten, wenn persistierende moderate/hohe Krankheitsaktivität (LINK zu DAS 28)
Schlechte Prognosefaktoren: ACPA/RF-Positivität, hohe Krankheitsaktivität, frühe Erosionen
Bei GUTER Prognose (keine Risikofaktoren):
Nutzung einer csDMARD Kombinationstherapie (z.B. MTX + Leflunomid) oder Wechsels der Basistherapie
Bei SCHLECHTER Prognose (≥1 Risikofaktor) oder fehlendem Ansprechen auf zwei csDMARDs:
csDMARD (i.d.R. MTX) + bDMARD/tsDMARD
tsDMARDs: Ggf. Risikofaktoren (MACE, maligne Erkrankungen, Thrombembolische Ereignisse beachten und therapieren
Januskinase-Inhibitoren (JAKi)
Cave: TNFi + Leflunomid werden in der Regel von der Krankenkasse als unwirtschaftlich angesehen und können zu Regeressen führen! Grundsätzlich ist eine Kombinationstherapie aber wirksam.
Bei unzureichendem Ansprechen oder Unverträglichkeit:
Wechsel auf ein alternatives bDMARD mit gleichem oder anderem Wirkprinzip oder auf ein tsDMARD.
Nochmaliger Wechsel ohne Änderung des Wirkprinzips ist nicht sinnvoll.
Bei Therapiebeginnen mit tsDMARD bei Nichtansprechen Wechsel auf ein bDMARD
Biologika (bDMARDs)
TNF-Inhibitoren: Adalimumab, Certolizumab, Etanercept, Infliximab, Golimumab
IL-6-Rezeptor-Antagonisten: Sarilumab, Tocilizumab
CTLA-4-Ig: Abatacept
B-Zell-Depletion: Rituximab
JAK-Inhibitoren (tsDMARDs): Baricitinib, Filgotinib, Tofacitinib, Upadacitinib
EULAR 2022: "after careful consideration of risks of MACEs, malignancies and/or thromboembolic events" - Tofacitinib, Baricitinib, Filgotinib, Upadacitinib
Erhöhte Vorsicht nach ORAL-Surveillance-Studie
Lebendimpfungen vor Immunsuppression
Pneumokokken, Influenza, Herpes zoster empfohlen
MTX und Leflunomid kontraindiziert
Leflunomid-Auswaschung vor geplanter Schwangerschaft (Cholestyramin)
Sulfasalazin, Hydroxychloroquin, Certolizumab empfohlen
Weitere Therapien möglich: EULAR recommendations for use of antirheumatic drugs in reproduction, pregnancy, and lactation: 2024 update - Annals of the Rheumatic Diseases
Definition: Chronisch-entzündliche Systemerkrankung mit bevorzugtem Befall der Synovialis Prävalenz:
Weltweite Prävalenz: ~1% der Bevölkerung - Geschlechtsverteilung: 2-3x häufiger bei Frauen
Lebenszeitrisiko: 2% (Männer), 4% (Frauen)
Symmetrische Polyarthritis kleiner Gelenke
Bevorzugter Befall: MCP-, PIP-Gelenke, Handgelenke - Symmetrisches Befallsmuster
Befall großer Gelenke V.a. bei fortgeschrittener Erkrankung
Morgensteifigkeit > 30 Minuten
Diagnostisches Leitsymptom der entzündlichen Arthritis, bei degenerativen Beschwerden typischerweise wenige Minuten
Dauer korreliert mit Krankheitsaktivität; Besserung im Tagesverlauf typisch
Allgemeinsymptome
Fatigue: Häufigstes Allgemeinsymptom
B-Symptomatik: Seltener, korrelierend mit systemischer Entzündung
Kardiovaskuläre Komorbidität durch systemische Inflammation
Klinisch: synovialitische Schwellung, Druckschmerz, Gelenkbefallsmuster
Synovitis-Nachweis als Grundvoraussetzung - Dokumentation von Schwellung und Druckschmerz
Funktionseinschränkung und Bewegungsumfang
Labordiagnostik: RF, ACPA, BSG/CRP
Rheumafaktor (RF): Klassischer Biomarker
ACPA (Anti-CCP): Höhere Spezifität, prognostisch relevant
Akute-Phase-Reaktanten: BSG/CRP für Aktivitätsbeurteilung
Bildgebung: Röntgen, Sonografie, MRT
Konventionelles Röntgen: Erosionsnachweis, Verlaufskontrolle
Sonografie: Synovitis-Nachweis, frühe Veränderungen
MRT: Höchste Sensitivität für frühe entzündliche Veränderungen
Klassifikationskriterien: ACR/EULAR 2010 (LINK zu Klassifikationskriterien)
Gelenkbeteiligung (0-5 Punkte)
Serologie (0-3 Punkte)
Akute-Phase-Reaktanten (0-1 Punkt)
Symptomdauer (0-1 Punkt)
EULAR – Management of Sjögren’s syndrome with topical and systemic therapies
https://ard.bmj.com/content/79/1/3
ACR/EULAR – 2016 Klassifikationskriterien für primäres Sjögren-Syndrom
https://ard.eular.org/article/S0003-4967(24)01570-X/fulltext
AWMF/DGRh – Diagnostik und Therapie der systemischen Sklerose
Übersicht https://register.awmf.org/de/leitlinien/detail/060-014
Langfassung https://register.awmf.org/assets/guidelines/060-014l_S2k_Diagnostik_Therapie_systemische_Sklerose_2025-07_1.pdf
EULAR – Treatment of systemic sclerosis (2023 update)
https://ard.eular.org/article/S0003-4967(24)00584-3/fulltext
ACR/EULAR – 2013 Klassifikationskriterien für systemische Sklerose
https://ard.bmj.com/content/72/11/1747
AWMF/DGRh – S3 Management des systemischen Lupus erythematodes inklusive sekundärem Antiphospholipid-Syndrom, Kinderwunsch und Schwangerschaft 2025
Übersicht https://register.awmf.org/de/leitlinien/detail/060-008
Langfassung https://register.awmf.org/assets/guidelines/060-008l_S3_Management-des-systemische-Lupus-erythematodes_2025-07.pdf
EULAR – Management of systemic lupus erythematosus (2023 update)
https://ard.bmj.com/content/83/1/15
ACR – Lupus Guideline Hub
https://rheumatology.org/lupus-guideline
ACR – 2025 Guideline for Systemic Lupus Erythematosus
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/acr.25690
ACR – 2024 Guideline for Lupus Nephritis
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/art.43212?af=R
EULAR/ACR – 2019 Klassifikationskriterien für SLE
https://pmc.ncbi.nlm.nih.gov/articles/PMC6827566/
ACR/EULAR – 2023 Klassifikationskriterien für APS
https://ard.eular.org/article/S0003-4967(24)10290-7/fulltext
DGRh – perioperativer Umgang mit Glukokortikoiden, DMARDs und Biologika
https://www.dgrh.de/lesen/empfehlungen/perioperativer-umgang/
DGRh – Impfungen bei entzündlich-rheumatischen Erkrankungen
https://www.dgrh.de/aktuelles/impfungen-bei-entzuendlich-rheumatischen-erkrankungen/
STIKO/RKI – Impfen bei Immundefizienz
https://www.rki.de/DE/Themen/Infektionskrankheiten/Impfen/Staendige-Impfkommission/Immundefizienz/immundefizienz-node.html
STIKO/RKI – Tabellenübersicht Impfen bei Immundefizienz
https://www.rki.de/DE/Themen/Infektionskrankheiten/Impfen/Staendige-Impfkommission/Empfehlungen-der-STIKO/Mitteilungen/Tabelle_Immundefizienz.html
ACR – Vaccinations in Patients With Rheumatic and Musculoskeletal Diseases (2022)
https://pmc.ncbi.nlm.nih.gov/articles/PMC10291822/
Überblick über die neuen EULAR-Empfehlungen zur antirheumatischen Therapie bei Kinderwunsch, in der Schwangerschaft und Stillzeit 2025
https://link.springer.com/article/10.1007/s00393-025-01727-8
EULAR recommendations for use of antirheumatic drugs in reproduction, pregnancy, and lactation: 2024 update
https://ard.eular.org/article/S0003-4967(25)00818-0/fulltext
EULAR recommendations for women's health and the management of family planning, assisted reproduction, pregnancy and menopause in patients with systemic lupus erythematosus and/or antiphospholipid syndrome
https://ard.bmj.com/content/76/3/476
ACR – Reproductive Health in Rheumatic and Musculoskeletal Diseases (2020)
https://rheumatology.org/reproductive-health-rheumatic-diseases-guideline
https://acrjournals.onlinelibrary.wiley.com/doi/10.1002/art.41191
